Fotodinamica: nuovo dispositivo impiantabile per terapia personalizzata
La terapia fotodinamica (PDT) è un esempio clinico in cui l’illuminazione ottica attiva selettivamente farmaci sensibili alla luce (fotosensibilizzanti), distruggendo le cellule tumorali senza effetti collaterali associati a trattamenti sistemici, come la chemioterapia. L’efficace applicazione clinica della PDT e di altre terapie a base di luce, tuttavia, dipende fortemente dalla somministrazione della luce attraverso il tessuto biologico che è otticamente opaco.
I recenti progressi nelle tecnologie wireless hanno consentito il controllo wireless dell’erogazione della luce direttamente alle cellule tumorali in vivo su modelli animali; questa versatilità nel nuovo metodo di erogazione estende la precisione spaziale e temporale della PDT alle regioni più profonde del corpo.
La terapia fotodinamica ad oggi
A differenza della chemioterapia, spesso somministrata in combinazione con la chirurgia e con possibili effetti collaterali tossici, la PDT colpisce specificamente le cellule tumorali riducendo al minimo i danni ai tessuti sani circostanti.
La terapia fotodinamica attualmente comporta la somministrazione di un farmaco fotosensibile, che viene assorbito e trattenuto nelle cellule tumorali; questo viene attivato per irradiazione con luce di una lunghezza d’onda specifica e rilascia specie reattive dell’ossigeno che uccidono le cellule tumorali circostanti.

Per colpire le regioni profonde, l’attuale PDT clinica utilizza fibre ottiche, ma la loro incompatibilità con l’impianto complessivo consente l’erogazione di una singola dose di luce per intervento chirurgico.
Gli hardware per la terapia fotodinamica attualmente esistenti soffrono di limitazioni chiave nel:
- erogazione della luce alle cellule tumorali profonde (ad esempio, i cavi fisici alle sorgenti luminose complicano l’accesso alle cellule tumorali nelle zone profonde interessate);
- controllo delle sorgenti luminose e/o delle lunghezze d’onda in modo programmato (ad esempio, le sorgenti luminose con lunghezza d’onda singola attiverebbero un fotosensibilizzatore a un ritmo modesto se un fotosensibilizzatore ha due picchi di assorbimento);
- multiplazione in modo che più tipologie di cellule possano essere trattate contemporaneamente.
Per superare questi problemi, un team di ricercatori ha progettato un dispositivo LED wireless a bassa potenza per l’attivazione del fotosensibilizzatore.
La svolta: un nuovo dispositivo impiantabile
Alcuni ricercatori hanno progettato un dispositivo optoelettronico impiantabile wireless in grado di fornire con efficacia la terapia fotodinamica alle cellule tumorali.
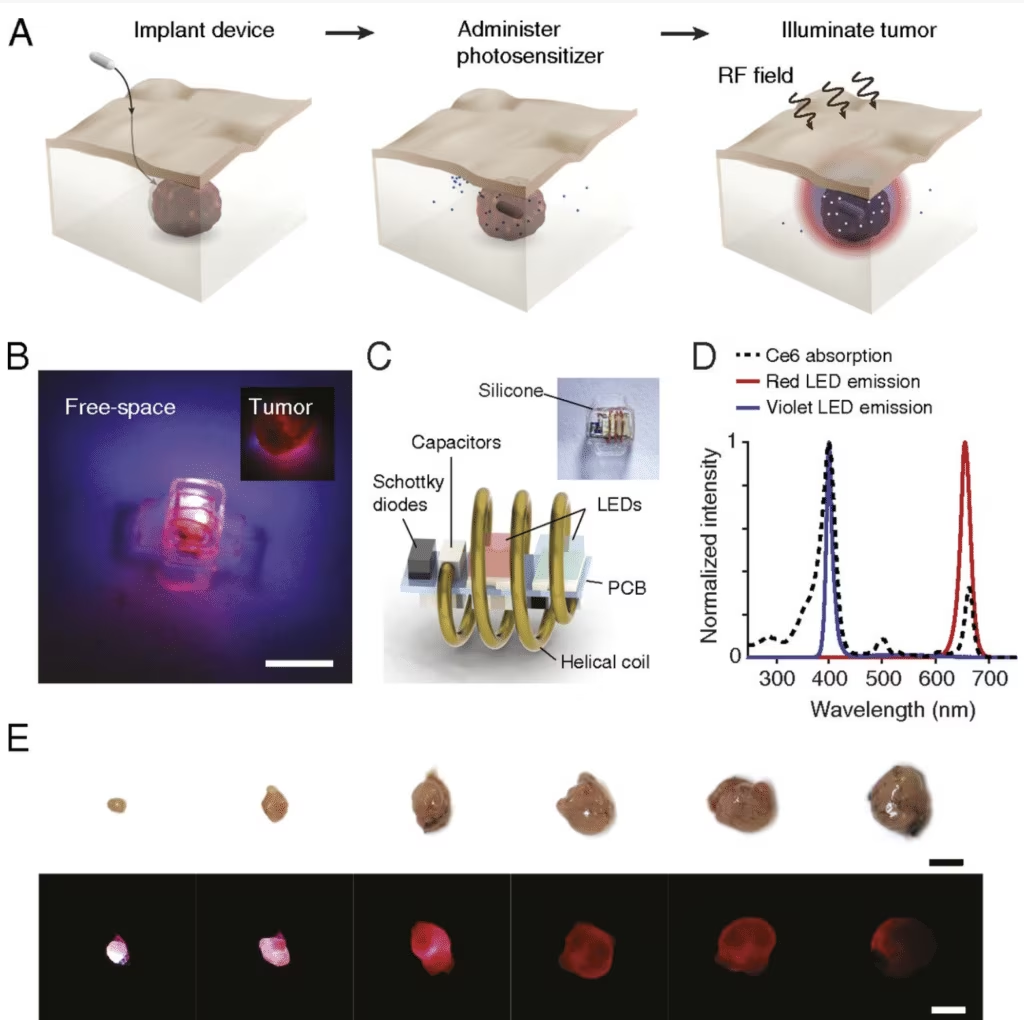
Il funzionamento del dispositivo è basato sull’algoritmo DeepLabCut (DLC), che stima le pose degli animali in movimento libero in tempo reale, e su una piattaforma di simulazione termica/luce, che simula le risposte dei fotosensibilizzanti alla luce ricevuta. Con questa combinazione di software, i ricercatori hanno dimostrato come i dispositivi impiantabili potrebbero essere adattati alle risposte dei singoli tumori.
A seconda delle dimensioni di un tumore e del fotosensibilizzatore usato per trattarlo, gli studi hanno mostrato come i dispositivi impiantabili su misura potrebbero essere ottimizzati per produrre una combinazione adeguata di sorgenti luminose e di lunghezze d’onda per massimizzare l’attivazione del fotosensibilizzatore.
Sperimentazioni e prospettive dello studio
I ricercatori hanno valutato le prestazioni del dispositivo utilizzando modelli murini di cancro del colon-retto, producendo una diminuzione fino al 76% del volume tumorale dopo cinque giorni di trattamento continuo con PDT a doppia lunghezza d’onda. Sulla base di questi risultati, hanno stabilito una nuova serie di linee guida per l’effettiva consegna di PDT.
Successivamente si è dimostrata l’efficacia del sistema di erogazione della luce per la PDT del cancro nei topi con l’inserimento del dispositivo impiantabile. Il monitoraggio del volume tumorale in funzione del tempo ha rivelato la soppressione, e in alcuni casi la completa regressione, dei tumori nel gruppo di topi trattati.

A lungo termine, il team spera che questa sperimentazione (in cooperazione con la terapia genica) in futuro possa migliorare le capacità di monitoraggio del cancro al di fuori delle strutture ospedaliere e all’infuori di laboratori attentamente controllati così da poter aiutare a prevenire il riemergere di tumori situati in qualsiasi parte del corpo, migliorando significativamente la qualità della vita delle persone che vivono con diverse tipologie di cancro.
